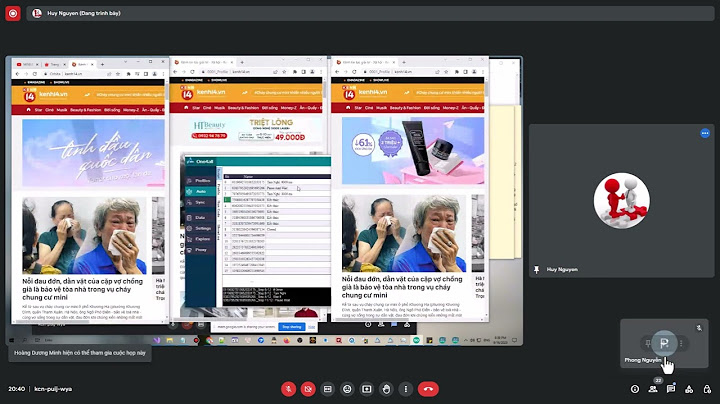
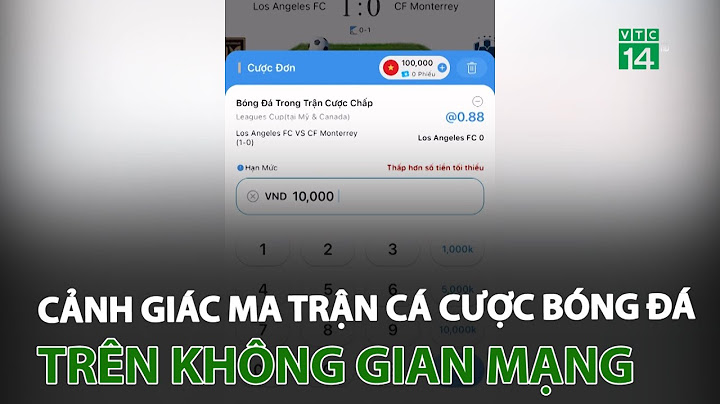
Cho phương trình hóa học của phản ứng: X +2Y → Z + T. Ở thời điểm ban đầu, nồng độ của chất X là 0,01 mol/l. Sau 20 giây, nồng độ của chất X là 0,008 mol/l. Tốc độ trung bình của phản ứng theo chất Y trong khoảng thời gian trên là:
Đáp án đúng: D Ta có: Nếu tính theo X: \(v = \frac{C_1 - C_2}{t}= 10^{-4}\) M/s Nhưng do hệ số của Y gấp 2 lần của X trong phương trình ⇒ vY = 2v = 2.10-4 M/s YOMEDIA Hướng dẫn Trắc nghiệm Online và Tích lũy điểm thưởng CÂU HỎI KHÁC VỀ TỐC ĐỘ PHẢN ỨNG VÀ CÂN BẰNG HÓA HỌC
Dưới đây là một vài câu hỏi có thể liên quan tới câu hỏi mà bạn gửi lên. Có thể trong đó có câu trả lời mà bạn cần!  Cho phương trình hóa học của phản ứng: X + 2 Y → Z + T Ở thời điểm ban đầu, nồng độ của chất X là 0,01 mol/l. Sau 20 giây, nồng độ của chất X là 0,008 mol/l. Tốc độ trung bình của phản ứng tính theo chất X trong khoảng thời gian trên là A. 4,0.10-4 mol/(l.s). B. 7,5.10-4 mol/(l.s). C. 1,0.10-4 mol/(l.s). D. 5,0.10-4... Đọc tiếp Cho phương trình hóa học của phản ứng: X + 2 Y → Z + T Ở thời điểm ban đầu, nồng độ của chất X là 0,01 mol/l. Sau 20 giây, nồng độ của chất X là 0,008 mol/l. Tốc độ trung bình của phản ứng tính theo chất X trong khoảng thời gian trên là
  14 tháng 2 2017 lúc 4:00 Đáp án C   Cho phản ứng hóa học: Br 2 + HCOOH → 2 HBr + CO 2 Lúc đầu nồng độ của HCOOH là 0,010 mol/l, sau 40 giây nồng độ của HCOOH là 0,008 mol/l. Tốc độ trung bình của phản ứng trong khoảng thời gian 40 giây tính theo HCOOH là A. 5,0.10-5 mol/(l.s). B. 2,5.10-5 mol/(l.s). C. 2,5.10-4 mol/(l.s). D. 2,0.10-4... Đọc tiếp Cho phản ứng hóa học: Br 2 + HCOOH → 2 HBr + CO 2 Lúc đầu nồng độ của HCOOH là 0,010 mol/l, sau 40 giây nồng độ của HCOOH là 0,008 mol/l. Tốc độ trung bình của phản ứng trong khoảng thời gian 40 giây tính theo HCOOH là
  4 tháng 1 2020 lúc 10:43 Đáp án A   Cho phản ứng A + B ⇄ C . Nồng độ ban đầu của chất A là 0,1 mol/l, của chất B là 0,8 mol/l. Sau 10 phút, nồng độ của B giảm 20% so với nồng độ ban đầu. Tốc độ trung bình của phản ứng là: A. 0,16 mol/l.phút B. 0,016 mol/l.phút C. 1,6 mol/l.phút D. 0,106... Đọc tiếp Cho phản ứng A + B ⇄ C. Nồng độ ban đầu của chất A là 0,1 mol/l, của chất B là 0,8 mol/l. Sau 10 phút, nồng độ của B giảm 20% so với nồng độ ban đầu. Tốc độ trung bình của phản ứng là:
  10 tháng 1 2017 lúc 14:49 Chọn B     8 tháng 11 2019 lúc 17:44 Chọn D Tốc độ trung bình của phản ứng tính theo chất B là:   Khi bắt đầu phản ứng, nồng độ một chất là 0,024 mol/l. Sau 10 giây xảy ra phản ứng, nồng độ của chất đó là 0,022 mol/l. Tốc độ trung bình của phản ứng trong trường hợp này là A. 0,00015 mol/l.s. B. 0,0003 mol/l.s. C. 0,0002 mol/l.s. D. 0,0004... Đọc tiếp Khi bắt đầu phản ứng, nồng độ một chất là 0,024 mol/l. Sau 10 giây xảy ra phản ứng, nồng độ của chất đó là 0,022 mol/l. Tốc độ trung bình của phản ứng trong trường hợp này là
  9 tháng 7 2017 lúc 2:47 Đáp án C    23. Một phản ứng có tốc độ phản ứng ở ở 50o C là 10−5 mol/l.s; ở 100o C, tốc độ phản ứng bằng 10−2 mol/l.s. Tính năng lượng hoạt hóa dựa vào phương trình Arrhenius. Cho biết R = 1,987 cal/mol.K. 24. Tính tốc độ trung bình của phản ứng, biết rằng khi bắt đầu phản ứng, nồng độ của một chất là 0,1 mol/l; sau 1 phút nồng độ của chất còn lại 0,05 mol/l. 25. Một phản ứng có hệ số nhiệt độ của... Đọc tiếp 23. Một phản ứng có tốc độ phản ứng ở ở 50o C là 10−5 mol/l.s; ở 100o C, tốc độ phản ứng bằng 10−2 mol/l.s. Tính năng lượng hoạt hóa dựa vào phương trình Arrhenius. Cho biết R = 1,987 cal/mol.K. 24. Tính tốc độ trung bình của phản ứng, biết rằng khi bắt đầu phản ứng, nồng độ của một chất là 0,1 mol/l; sau 1 phút nồng độ của chất còn lại 0,05 mol/l. 25. Một phản ứng có hệ số nhiệt độ của tốc độ phản ứng bằng 3,33. Ở 25°C, phản ứng kết thúc sau 2 giờ. Dựa vào quy tắc thực nghiệm Van’t Hoff, cho biết sau bao lâu phản ứng kết thúc nếu tiến hành phản ứng ở 80°C. giúp các ậu ạ   4 tháng 6 2020 lúc 8:55 Câu 23 bạn tự áp vào công thức là tính ra Ea thôi. Nên em tự làm nhé Câu 24: \(\overline{v}=\frac{\left|\Delta C\right|}{\Delta t}=\frac{0,05}{1}=0,05M.phút^{-1}\) Câu 25 vsau = vtrước.3,33(80-25):10= 747.vtrước \=> Thời gian thực hiện pứ = 2/747 giờ    3 tháng 9 2023 lúc 18:47
Trong đó k là hằng số tốc độ phản ứng CX.CY lần lượt là nồng độ của X và Y tại một thời điểm đang xét b) - Tốc độ phản ứng tại thời điểm đầu: v = k . CX.CY = 2,5 . 10-4 . 0,02 . 0,03 = 1,5 . 10-7(mol/(Ls)) - Tốc độ phản ứng tại thời điểm hết một nửa lượng X \=> CX= 0,01 M CY = 0,02 M v = k . CX.CY = 2,5 . 10-4 . 0,01 . 0,02 = 5.10-8(mol/(Ls))  Cho phản ứng: A + B D C Nồng độ ban đầu của A là 0,1 mol/1, của B là 0,8 mol/l. Sau 10 phút, nồng độ của B chỉ còn 20% nồng độ ban đầu. Tốc độ trung bình của phản ứng là: |